1. 洗浄評価を実施したきっかけ
1-1. 出ていると思っていた超音波がインジケータで検出されなかった
今回、当院が洗浄評価を実施してみようと思った直接的なきっかけは、超音波インジケータの変色不良でした。
当院のWDには超音波洗浄機能がついており、以下の2つのプログラムを使用しています。洗浄の難易度が高いものについては、超音波洗浄がある「プログラム2」を適応しています。
プログラム1:洗浄50℃ 10分(超音波なし)
プログラム2:洗浄50℃ 5分、超音波洗浄 40℃ 10分
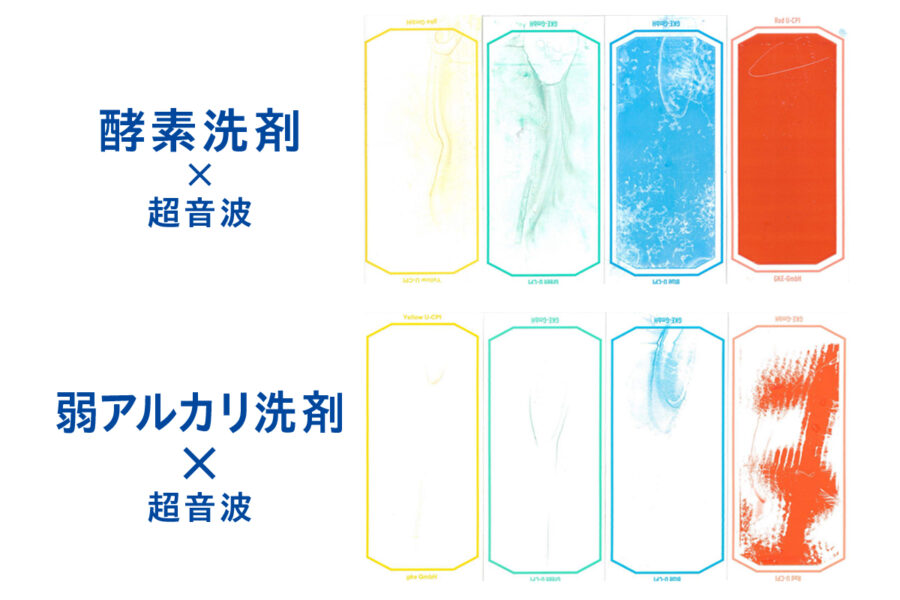
ある日、ふと当院のWDの超音波が適切に機能しているのか気になり、超音波のみを検出するタイプの市販のインジケータを試したところ、インジケータが変色しない、という結果が得られました。超音波が出ていそうな音はしていますが、「実は超音波が出ていないのでは?」と疑問を持つようになりました。
1-2. 洗浄器の部品交換にはそれなりのコストがかかる
すぐに洗浄器メーカーに相談したところ、超音波の性能は経年劣化していくものであり、法定の耐用年数は4年であることがわかりました。当院の洗浄器は購入後すでに7年が経過しており、修理などでその性能を戻すことは難しく、振動子や発振器の交換が必要という回答が得られました。
ただ、部品交換にはそれなりのコストがかかります。すぐに予算を獲得するのも難しい状況であったため、超音波に頼らない洗浄工程を模索することにしました。
1-3. バリデーション(PQ)実施のハードルは高い
再生処理に関わる私たちは、洗浄および滅菌におけるバリデーション(PQ)を実施しなければなりません。洗浄工程を変更する場合も、新たな工程が適切に洗浄できるものであるかを検証する必要があります。しかし、これらをきちんと実施できている医療機関は少ないのではないでしょうか。
『医療機器学』に掲載されている「滅菌保証に関する実態調査報告6」では、当院のような中小規模の病院でバリデーションを実施している施設は4割以下であることがわかっています。そのほとんどは、バリデーションの必要性自体は認識していました。
〔アンケート〕バリデーションの必要性について
出典:『医療機器学』93 巻 (2023) 4 号「滅菌保証に関する実態調査報告6」
バリデーションを行わない理由としては、「実施方法がわからない」「時間的余裕がない」「必要な器具や設備がない」「予算を確保するのが困難」といった理由が挙げられています。特に中小規模の病院においては、中央材料室に対する投資に消極的である場合も多く、バリデーション実施のハードルは高いのでは、と感じています。
〔アンケート〕バリデーションを行わない理由
出典:『医療機器学』93 巻 (2023) 4 号「滅菌保証に関する実態調査報告6」
1-4. 今回の検証では洗浄評価を実施
ウォッシャーディスインフェクター(WD)の工程は、予備洗浄→洗浄→すすぎ→熱水消毒→乾燥の5つがあります。『医療現場における滅菌保証のガイドライン2021』(以下ガイドライン)では、この5つの工程に対して、①残留蛋白質の測定、②すすぎ性の確認、③熱水消毒効果の確認、④乾燥性能と製品適格性の確認、の4つを実施することが勧告されています。

これらの手順は煩雑で、中小規模の病院ですべての検証を行い評価することは、なかなか大変です。ですので、まず今回は、これらの中で感染に直結する①残留蛋白質の測定(洗浄評価)を実施してみることにしました。
1-5. 洗浄評価の基準値は、残留蛋白質量200μg/RMD以下
器材が適切に洗浄できているかの基準について、ガイドラインでは洗浄後の器材に残留する蛋白質量が200μg/RMD以下であることが目標数値となっています。
8.2 洗浄評価基準
(勧告)
洗浄後のRMDに残留する蛋白質量が、200μg/RMD以下であることを確認する出典:『医療現場における滅菌保証のガイドライン2021』p.100
1-6. 洗浄評価と合わせて洗浄インジケータの選定も実施した
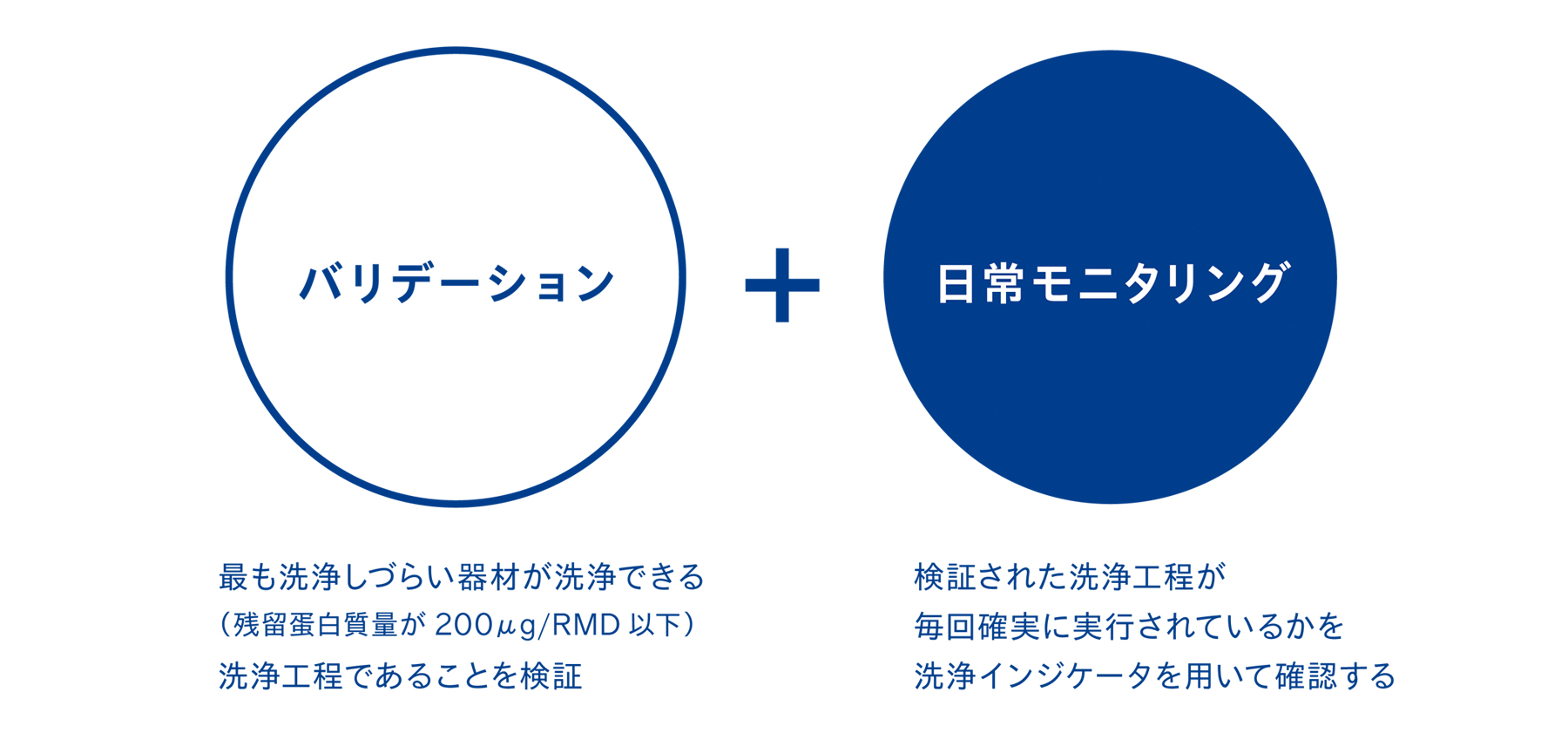
洗浄工程の評価は、「洗浄評価+日常モニタリング」で考えるのが基本です。洗浄評価された洗浄工程が、毎回確実に実行されているかを洗浄インジケータを用いて確認することで保証します。今回の検証では、洗浄評価の実施に合わせて適切な洗浄インジケータの選定試験も行いました。
2. 洗浄評価の実施内容
本章では、今回実施した洗浄評価で使用した洗浄器やマスター製品、実施の流れをご紹介します。
2-1. 洗浄条件
当院では、サクラ精機社のWUS-2100に、サラヤ社のパワークイック(アルカリ)を使用しています。洗浄評価を実施したプログラムは以下の2つです。
プログラム1:洗浄50℃ 10分(超音波なし)
プログラム2:洗浄50℃ 5分、超音波洗浄40℃ 10分

(当日のスライドより)
2-2. マスター製品の選定
洗浄評価では、もっとも洗浄が難しいマスター製品を選定し、その残留蛋白質量が200μg/RMD以下になるかを検証します。ガイドラインでは、マスター製品を以下の表に基づいて選定するよう記載されています。

(当日のスライドより)
当院では、整形外科の器材がマスター製品候補となりましたが、バリエーションの多い外傷手術からまとまった数の器材を用意するのは非現実的という課題がありました。
そこで今回は、ガイドラインの選定方法に従い、止血鉗子を暫定的なマスター製品とすることにしました。止血鉗子などの鉗子類は、パーツが交差する構造となっていますが、この交差部分をボックスロックと言います。ボックスロックは、器材の構造でもっとも洗浄されにくい箇所と言われており、この部分で残留蛋白質が200μg以下であれば、他の部分も適切に洗浄されていると考えます。

(当日のスライドより)
またこのような止血鉗子については、ガイドラインに準拠して作成された疑似血液が塗布されているテストデバイスが市販されています。今回は、サラヤ社のテストデバイスを洗浄評価に使用しました。
このテストデバイスは、疑似汚染物である羊の血液を止血鉗子のボックスロック部に100μL滴下し、ボックスロック部に浸透するよう数回開閉。その後デバイスを45度に開いた状態で1時間乾燥させた後、真空パックに梱包されたものです。

(当日のスライドより)
2-3. 積載方法
次に、洗浄槽内への積載方法の設定です。当院では、トレイや膿盆、カップ、シャーレなどを洗浄する場合は、超音波洗浄の際に下からも水が出るため、上段への水流を妨げないよう上段に配置しています。中段と下段には、鉗子類を積載しています。

(当日のスライドより)
2-4. 洗浄評価の流れ
テストデバイスを用いた洗浄評価は、以下の流れで実施します。
① 疑似汚染物が塗布されたテストデバイスを使用する分だけ開封する
② テストデバイスと他の器材を洗浄バスケットにセットし積載する
③ 洗浄器の運転を開始する
④ すすぎが終了したタイミングでプログラムを途中停止し、テストデバイスを取り出す
⑤ テストデバイスを3回開閉させ、残渣がないかを目視で確認する
⑥ 清浄な環境で自然乾燥させる
⑦ 乾燥後、再度残渣がないかを目視で確認する
⑧ テストデバイスを専用のバックに入れてメーカーへ着払いで発送する
⑨ 2週間ほどで、メーカーから残留蛋白質量に関する試験結果が届く

簡単に言えば、届いたデバイスを洗浄して、残渣を目視で確認して、返送するだけです。ちょっと、できそうな気がしませんか?
3. 洗浄評価の検証結果
3-1. 検証試験の全体像
今回の検証試験では、洗浄プログラムごとや洗浄に関する諸条件を変化させた時に残留蛋白質量がどのように変化するかを検証するため、以下のような比較検証を実施しました。
| 比較した内容 | プログラム | 洗浄 | 超音波 | 洗浄剤 |
| ①超音波あり vs 超音波なし | 超音波あり | 50℃ 5分 | 40℃ 10分 | アルカリ0.3% |
| 超音波なし | 50℃ 10分 | – | アルカリ0.3% | |
| ②浸漬あり vs 浸漬なし | 浸漬あり | 50℃ 10分 | – | アルカリ0.3% |
| 浸漬なし | 50℃ 10分 | – | アルカリ0.3% | |
| ③洗浄剤0.3% vs 洗浄剤0.5% | 洗浄剤0.3% | 50℃ 10分 | – | アルカリ0.3% |
| 洗浄剤0.5% | 50℃ 10分 | – | アルカリ0.5% | |
| ④50℃10分 vs 55℃15分 | 50℃10分 | 50℃ 10分 | – | アルカリ0.3% |
| 55℃15分 | 55℃ 15分 | – | アルカリ0.3% |
次項より、それぞれの検証試験の結果を紹介します。
3-2. ①超音波あり vs 超音波なし
今回洗浄評価を行うきっかけとなった超音波インジケータの変色不良により、すでに洗浄器の超音波機能が低下していることがわかっていたため、超音波の有無で残留蛋白質量にどの程度影響を与えるのかを検証しました。
超音波ありのプログラム2は、洗浄50℃ 5分+超音波40℃ 10分。超音波なしのプログラム1は、洗浄50℃ 10分です。この2つのプログラムで、テストデバイスを洗浄した時の残留蛋白質量を比較しました。

(当日のスライドより)
実際の残留蛋白質量の結果はこちらです。超音波ありのプログラム2では、目視による残渣(-*)は15本中1本。超音波なしのプログラム1では、残渣は15本中4本という結果になりました。残渣が認められず、残留蛋白質量の測定が可能であったデバイスについては、大きな差は認められませんでした。
| プログラム | 鉗子No. | 1回目 | 2回目 | 3回目 |
|
超音波あり |
① | <20.0 | 40.4 | 46.9 |
| ② | <20.0 | 36.7 | 41.2 | |
| ③ | <20.0 | 26.5 | <20.0 | |
| ④ | <20.0 | 53.0 | ―* | |
| ⑤ | <20.0 | 22.4 | 33.5 | |
| 超音波なし (洗浄50℃ 10分) |
① | 55.3 | ―* | 42.5 |
| ② | ―* | 31.1 | <20.0 | |
| ③ | ―* | 45.3 | 25.0 | |
| ④ | 45.6 | <20.0 | ―* | |
| ⑤ | 20.0 | 20.4 | 46.6 |
3-3. ②浸漬あり vs 浸漬なし
当院では、洗浄の難易度が高い器材を洗浄する時は、洗浄器に入れる前に浸漬洗浄を実施しています。そこで、超音波なしのプログラム1において、事前に浸漬洗浄をした場合としなかった場合の残留蛋白質量の比較を行いました。

(当日のスライドより)
残留蛋白質量の結果はこちらです。浸漬ありは残渣が15本中3本、浸漬なしは15本中4本でした。残渣が認められず、残留蛋白質量の測定が可能であったデバイスについては、浸漬ありの方が残留蛋白質量が比較的少ないという結果になりました。
| プログラム | 鉗子No. | 1回目 | 2回目 | 3回目 |
|
浸漬あり |
① | ―* | <20.0 | 21.9 |
| ② | 35.2 | 23.3 | 23.6 | |
| ③ | <20.0 | <20.0 | ―* | |
| ④ | <20.0 | <20.0 | 21.0 | |
| ⑤ | 52.0 | 34.8 | ―* | |
| 浸漬なし (洗浄50℃ 10分) |
① | 55.3 | ―* | 42.5 |
| ② | ―* | 31.1 | <20.0 | |
| ③ | ―* | 45.3 | 25.0 | |
| ④ | 45.6 | <20.0 | ―* | |
| ⑤ | 20.0 | 20.4 | 46.6 |
3-4. ③洗浄剤0.3% vs 洗浄剤0.5%
これまでの検証において、どのプログラムでも残渣が発生したため、残渣をなくすための洗浄工程の改善を試みました。まずは、投入する洗浄剤の濃度を変えて比較してみることにしました。
当院で使用しているサラヤのパワークイックは、推奨濃度が0.5%、器材に応じて0.2~0.5%で調整可能と記載されています。当院では、長年0.3%の濃度で運用してきましたが、誰がどのように決定したのか不明であったため、今回濃度0.5%でも検証してみることにしました。

(当日のスライドより)
洗浄剤0.3%では残渣は15本中4本、0.5%では6本でした。また、残渣が認められず残留蛋白質量の測定可能なデバイスについても、その数値に大きな差は見られませんでした。必ずしも、洗浄剤の濃度が高ければ良いという訳ではないことがわかります。
| プログラム | 鉗子No. | 1回目 | 2回目 | 3回目 |
|
洗浄剤0.3% |
① | 55.3 | ―* | 42.5 |
| ② | ―* | 31.1 | <20.0 | |
| ③ | ―* | 45.3 | 25.0 | |
| ④ | 45.6 | <20.0 | ―* | |
| ⑤ | 20.0 | 20.4 | 46.6 | |
|
洗浄剤0.5% |
① | ―* | 29.7 | 27.1 |
| ② | 61.3 | ―* | 34.1 | |
| ③ | 47.5 | ―* | ―* | |
| ④ | ―* | 40.4 | ―* | |
| ⑤ | 40.4 | 23.0 | 41.5 |
3-5. ④50℃10分 vs 55℃15分
洗浄剤の濃度を高くしても残渣が残ったため、洗浄の温度と時間を調整し改善を試みました。
当院では通常、50℃10分にて洗浄していますが、温度を55℃まであげ、洗浄時間も15分まで延ばして検証しました。本来は洗浄時間を1分ずつ延ばしていけば良いですが、今回は検証期間も限られていたため、サラヤさんからの他施設の事例情報を参考に15分としました。

(当日のスライドより)
50℃10分のプログラムでは15本中4本に残渣が発生しましたが、55℃15分では残渣は発生しませんでした。また、55℃15分ではすべてのデバイスが200μg以下であり(平均46.8μg)、適切に洗浄できるプログラムであることが確認できました。
| プログラム | 鉗子No. | 1回目 | 2回目 | 3回目 |
|
50℃ 10分 |
① | 55.3 | ―* | 42.5 |
| ② | ―* | 31.1 | <20.0 | |
| ③ | ―* | 45.3 | 25.0 | |
| ④ | 45.6 | <20.0 | ―* | |
| ⑤ | 20.0 | 20.4 | 46.6 | |
|
55℃ 15分 |
① | 134.8 | 79.9 | 51.4 |
| ② | 52.6 | 35.4 | 43.8 | |
| ③ | 31.7 | 28.6 | 22.8 | |
| ④ | 28.7 | 67.6 | 30.0 | |
| ⑤ | 26.9 | 47.9 | <20.0 |
3-6. 洗浄評価の結果を踏まえて
これらの検証結果を踏まえて、当院では超音波つきのプログラムの使用は止め、超音波なしのプログラムの洗浄を55℃15分に変更することにしました。
4. 洗浄インジケータの選定
今回の検証試験では、テストデバイスによる洗浄評価の実施と合わせて、日常モニタリングに使用する適切な洗浄インジケータの選定も行いました。本章では、洗浄インジケータの選定についてご紹介します。
4-1. 洗浄器では検知できないエラーがある
最新の洗浄器では、洗浄剤が適切に投入されていないとセンサーが反応してエラーを出す機種が増えてきています。洗浄剤に限らず、機械洗浄ではさまざまなエラーが発生しますが、それらの中には洗浄器の機種によっては検知できないものもあります。
洗浄器では気づけないエラーを検知することが、洗浄インジケータを使用する大きな目的です。

(当日のスライドより)
4-2. 洗浄インジケータに関するガイドラインの記載
ガイドラインでは、日常の監視項目の1つとして洗浄インジケータの使用が勧告されています。
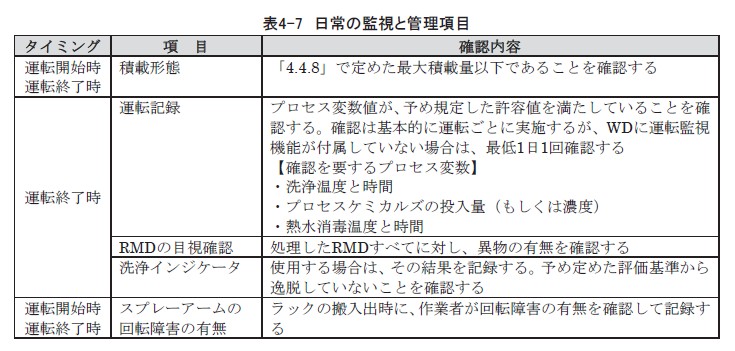 出典:『医療現場における滅菌保証のガイドライン2021』p.60
出典:『医療現場における滅菌保証のガイドライン2021』p.60
しかし、同時に「市販の洗浄インジケータは国内外の規格および推奨されているものはなく、メーカ独自のコンセプトで設計開発されている」とも記載されています(p107)。結局どの洗浄インジケータを使ったらいいのか判断ができず、困っていらっしゃる方もいるのではと思います。
4-3. SALWAY 洗浄工程インジケータ
今回は、当院の洗浄プラグラムに適したインジケータを選択するために、種類が一番多かったSALWAY の洗浄工程インジケータから選定してみることにしました。SALWAYの洗浄工程インジケータは、5色の異なる抵抗性(落ちづらさ)を持つインジケータから、自院のWDやプログラムに適したものを選択することができます。

4-4. 洗浄インジケータ選定のポイント
洗浄インジケータを使用する目的は、洗浄工程になんらかの不具合が発生し、洗浄力が低下した時にそれを確実に検知することです。そのためには、使用している洗浄器が本来もつ洗浄力に最も近い抵抗性をもつインジケータを選択する必要があります。
例えば、下図の例であれば、WD①では赤色のインジケータまで落とすことができます。もちろん、青色や黄色のインジケータも難なく色落ちします。では、WD①で黄色のインジケータを選択し、日常モニタリングを行ったらどうなるでしょうか。
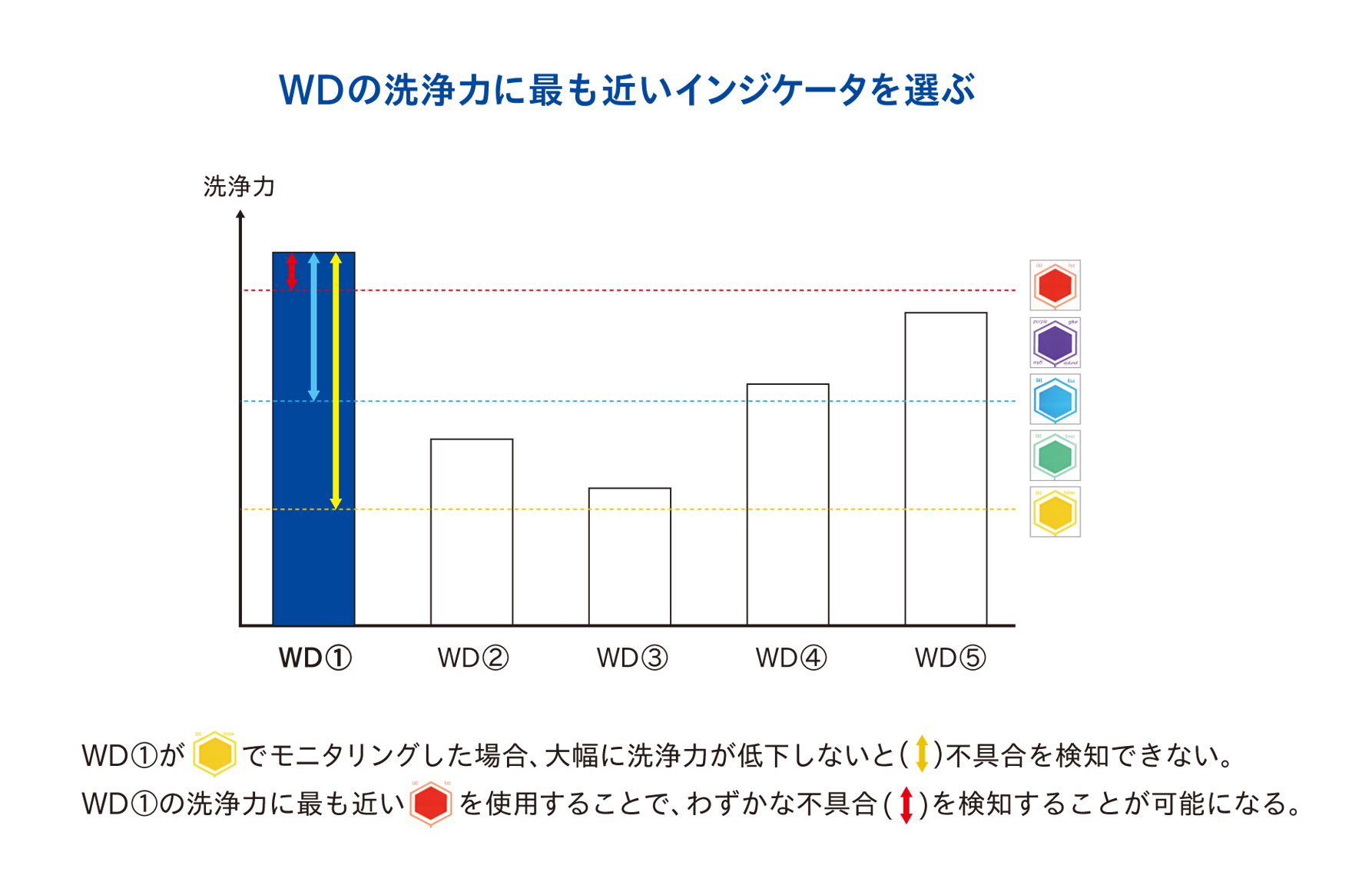
何らかの理由で、WDの洗浄力が大幅に落ちて半分程度になったとしても、黄色のインジケータは色落ちしてしまうため気づくことができません。なので、WD①には赤色のインジケータが良いということになります。WD④であれば青色、WD③であれば黄色が選択されることになります。
4-5. 洗浄インジケータの選定試験の結果
テストデバイスを用いた洗浄評価の結果により改善した洗浄プログラム1(55℃15分、アルカリ洗剤0.3%)において、適切な洗浄インジケータの選定試験を行いました。洗浄インジケータの色落ち結果がこちらです。

当院の洗浄器では、緑色が毎回きれいに色落ちし、青色は一部まだらに色が残る結果となりました。当院では、緑色の洗浄インジケータで日常モニタリングを実施することにしました。
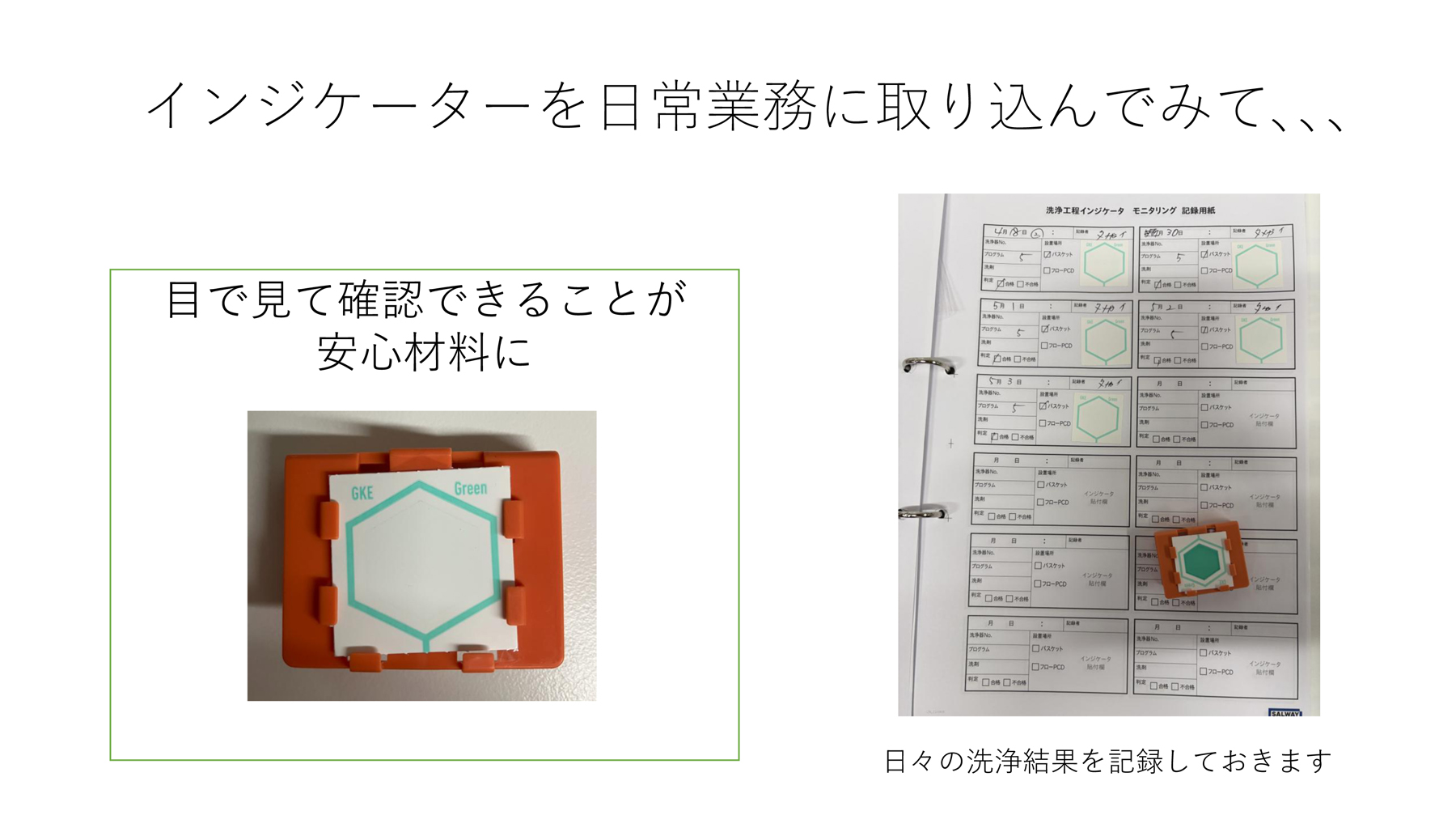
(当日のスライドより)
4-6. 不合格試験の結果
皆さんは不合格試験という言葉を聞いたことがありますか?不合格試験とは、あえて悪い結果が出るような条件で行う試験のことです。
例えば、洗浄器が正しく動作しなかった場合。洗浄インジケータがどのように色落ちするのか、不具合を適切に検知できるのかを検証するために行います。今回の検証試験においても、洗浄剤が供給されないことを想定した不合格試験を実施しました。
【試験条件】
55℃15分 アルカリ洗剤0%
不合格試験時の洗浄インジケータの色落ち結果はこちらです。先ほどは綺麗に色落ちしていた緑色も、全く色落ちしませんでした。

また、不合格試験時のテストデバイスの残留蛋白質量は以下の通りでした。テストデバイス15本中9本に残渣が確認され、適切に洗浄できていないことがわかります。
| プログラム | 鉗子No. | 1回目 | 2回目 | 3回目 |
|
不合格試験 |
① | 135.5 | 159.3 | ―* |
| ② | ―* | ―* | 146.5 | |
| ③ | 70.0 | ―* | 138.7 | |
| ④ | ―* | ―* | ―* | |
| ⑤ | 108.0 | ―* | ―* |
これらの検証試験の結果により、緑色の洗浄インジケータで日常モニタリングを行い、その変色が悪い時には器材も適切に洗浄できていない可能性が極めて高い、ということがわかるようになりました。
5. コスト削減の可能性
最後に、今回の検証を通じて感じたコスト削減の可能性についてお話しします。
5-1. 洗浄評価にはコストがかかる
洗浄評価にはコストがかかります。テストデバイスも購入する必要がありますし、日常的に洗浄インジケータも使いたい。しかし、残念ながら中央材料室はお金を生み出すことができない部門です。そして、洗浄や滅菌を正しく行うことを声高に訴えても、悔しい思いをしなくてはならないこともあります。

(当日のスライドより)
5-2. 洗浄評価によりコストを削減できる可能性がある
本来であれば、洗浄評価や日常モニタリングにかかる費用は、安全な手術を行うための必要な経費です。そこで、追加の予算が確保できないのであれば、自分たちで工夫してその分のコストを捻出することはできないかと考えました。
今回の洗浄評価の結果を受けて、経年劣化により性能が低下した超音波を使用しなくても、適切に洗浄できることがわかりました。当院では、平均すると1日あたり3回洗浄器を運転し、うち2回は超音波の洗浄プログラムを使用していました。超音波を使用すると、超音波なしのプログラムと比較して、一回あたり水量は95L、洗浄剤は90ml多く使用します。
あくまで試算ですが、変更後のプログラムで運用をすることで、材料費で約56,000円/年、人件費にして約400,000円/年の費用を捻出できる可能性があることがわかりました。このようにして浮かせた費用や時間で、洗浄評価や日常モニタリングを実施することもできるのではないでしょうか。
5-3. 安全な医療器材の提供はプライスレス
しかし、こういった直接的な費用だけの話ではありません。もし、洗浄や滅菌が不十分であれば、患者さんはどうなるでしょうか?
予想しない感染が発生するかもしれません。入院期間が伸びるかもしれません。抗菌薬も長期間使用しないとならないかもしれません。なにより、患者さんが苦しむかもしれません。
必要な検証の費用を惜しんでいては、もっと大きな影響が発生する可能性があります。40~50万円どころの話ではありません。患者さんに安全な医療器材を提供することは、プライスレスなんです。
6. 最後に伝えたいこと
私たちの仕事は、表にでませんし、なかなか評価されないこともあります。しかし、私たちの仕事の先には「患者さんの命」があります。
本日、私のつたないお話しを聴きに来てくださった皆さま。本当に有難うございました。一緒に頑張りましょう。