1. 日常の出荷判定用テストパック(PCD)とは?
1-1. その回の滅菌が正しく実施されたかを確認する器具
医療機関の再生処理業務では、再生処理によって安全な状態になった器材を「出荷(払い出し)」しています。この出荷では、適切に滅菌できているかを判定し、合格したものだけを払い出します。その判定のために使用するのが、「出荷判定用テストパック」と呼ばれるテスト器具です。出荷判定用テストパックは、各社から様々な製品が販売されています。
1-2. 抵抗性を持った構造とインジケータ(BIやCI)で構成される
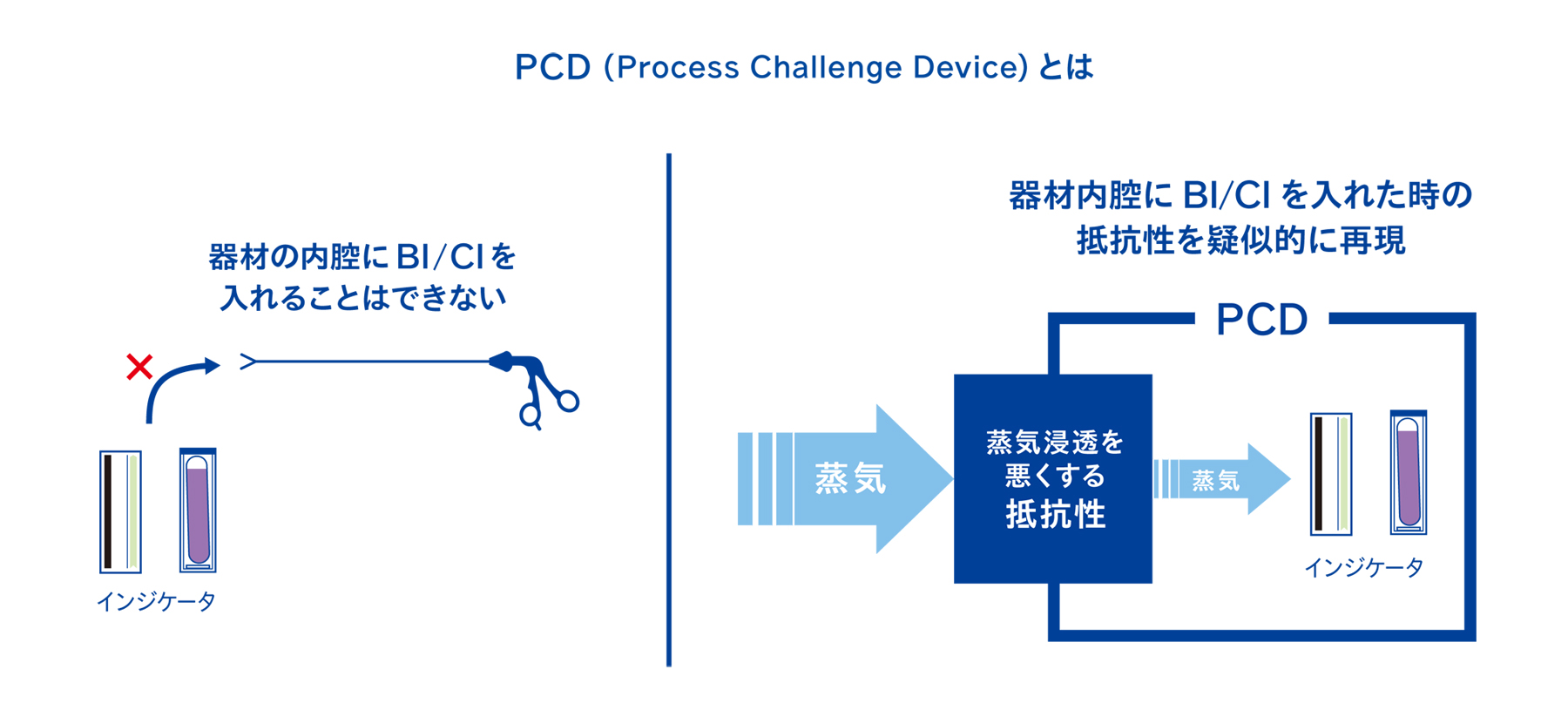
PCDは、意図的に蒸気浸透性を悪くする抵抗性を持った構造と、インジケータ(BIやCI)で構成されます。インジケータ単独ではなく、抵抗性を持った構造である理由は、インジケータだけでは管腔構造など複雑な構造を持った器材の滅菌確認ができないからです。
ラパロ鉗子の内側など、内腔構造の内側は器材の外側より蒸気が浸透しづらく、滅菌が困難です。滅菌が難しい器材内部までの滅菌条件の達成を確認するためには、本来はインジケータを器材内部に入れなくてはいけません。しかし、物理的にBIやCIを器材内部に挿入することはできません。そのため、器材内部のように滅菌がしづらい環境を疑似的に再現する構造が必要となるわけです。
1-3. PCDにはポーラス型とホローロード型の2種類がある
PCDは、積層構造のポーラス型と、内腔構造のホローロード型の2種類があります。
ポーラス型は、タオルや紙を積み重ねることで蒸気を浸透しづらくし、滅菌抵抗性をつくり出します。ホローロード型は、ラパロ鉗子や気腹チューブなどの内腔器材を模した内腔構造で滅菌抵抗性をつくり出します。
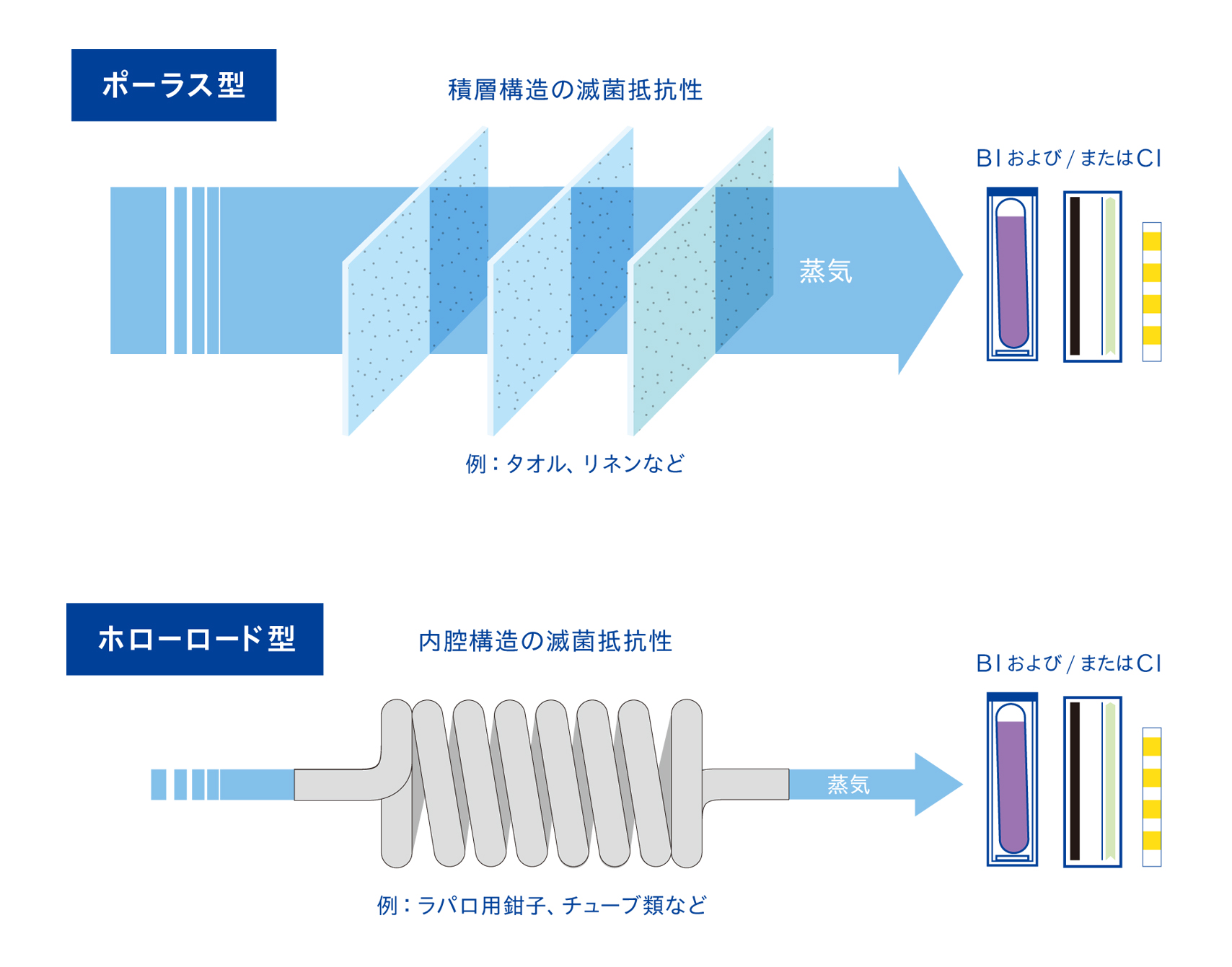
ポーラス型とホローロード型では、滅菌抵抗性が異なります。また、同じタイプでもメーカーによって準拠している規格が異なる場合があり、滅菌抵抗性はさまざまです。
1-4. 前提として滅菌物を全品検査することは出来ない
出荷判定用テストパック(PCD)を使用する背景には、滅菌したすべての器材の滅菌可否を確認することはできないという前提があります。滅菌したすべての器材を確認する時間もありませんし、そもそも包装材を開封してしまった時点で、その器材の無菌性は破綻してしまいます。
1-5. 出荷判定はワーストケースで考える
出荷判定は、ワーストケースを基準に合格・不合格を判定します。「最も条件が悪い器材が合格していれば、他の器材も合格している」と判断する考え方です。
滅菌におけるワーストケースは、「置かれる場所」と「器材の構造」の2つの要素があります。「置かれる場所」は、滅菌器のもっとも滅菌しづらい場所であること(コールドスポット)、「器材の構造」は、マスター製品よりも滅菌抵抗性が高く、滅菌が難しい構造であること(PCD)です。
コールドスポットでPCDが合格していれば、全ての器材は滅菌できていると推定します。

2. ガイドラインにおける出荷判定用テストパック(PCD)に関する記載
2-1. マスター製品と同等以上の滅菌抵抗性があるPCDを使用する
出荷判定用テストパック(PCD)について、『医療現場における滅菌保証のガイドライン2021』には以下のように記載されています。
『医療現場における滅菌保証のガイドライン2021』(p18)
日常の滅菌処理に使用する出荷可否判定用のテストパックは、以下の優先順位で選定する。①マスター製品にBIおよび/またはCIを設置したもの、②マスター製品に特性が似た製品や模擬製品にBIおよび/またはCIを設置したもの、③市販のPCDにBIおよび/またはCIを設置したもの。②または③を使用する時には、これらが①と同等以上の滅菌抵抗性であることの確認が必要である。
市販のPCDを日常の出荷判定に使用する場合は、マスター製品(滅菌する器材の中で最も滅菌しづらいもの)と同等以上の滅菌抵抗性を持ったPCDを選択する必要があります。
つまり、普段滅菌している滅菌物よりも滅菌抵抗性が低いPCDは、日常の出荷判定には使用できないということです。
2-2. PCDにBIおよび/またはCIを設置したものを使用する
市販のPCDの中に設置するインジケータについては、以下のように記載されています。
『医療現場における滅菌保証のガイドライン2021』(p18)
日常の滅菌処理に使用する出荷可否判定用のテストパックは、以下の優先順位で選定する。①マスター製品にBIおよび/またはCIを設置したもの、②マスター製品に特性が似た製品や模擬製品にBIおよび/またはCIを設置したもの、③市販のPCDにBIおよび/またはCIを設置したもの。②または③を使用する時には、これらが①と同等以上の滅菌抵抗性であることの確認が必要である。
ガイドライン2021では上記のような記載に留まっており、日常の出荷判定用テストパックにBIとCIのどちらを使用したらいいのかは明記されていません。
2-3. 国際規格ISO17665-2においても「CIおよび/またはBI」と記載とされている
国際規格ISO17665-2(ヘルスケア製品の滅菌 -湿熱-)の11章 “Product release from sterilization” においても、滅菌物の出荷について「CIおよび/またはBI」と記載されています。
If chemical indicators and/or biological indicators are used routinely, they should be treated as part of the release criteria and should be additional to the measurement of process parameters.
3. 検証試験の内容
3-1. 実際のマスター製品と市販のPCDの滅菌抵抗性を比較
今回は、実際のマスター製品と市販のPCDの滅菌抵抗性を比較する検証試験を実施しました。滅菌器の真空工程を調整し意図的に滅菌条件を悪くしていった時に、マスター製品と市販のPCDのどちらが先に不合格を示すかを検証しました。
3-2. マスター製品:重量11.3kgのコンテナに入れた疑似ラパロ鉗子
本試験では、トレイ・コンテナ含めて重量11.3kgのコンテナに、代表的な内腔器材であるラパロ鉗子を模した金属筒(直径8mm×長さ37.5cm)を入れ、それをマスター製品として設定しました。
これはAAMI包装器材PCD(ANSI/AAMI ST8:2013⁹⁾)をベースに、滅菌が困難な内腔器材の代表であるラパロ鉗子を加え、より厳しい条件にしたものです。
(ANSI/AAMI ST8:2013⁹⁾)
1)トレイも含めたPCD全重量は11.3kg以上とする.
2)包装器材PCDは以下で構成される.
a)いろいろな金属製手術用器具
b)穴あき,またはメッシュ底の約25cm×51cmの100%木綿製の手術用タオルを敷いたトレイ
c)少なくとも二つのBI
d)137cm×137cmの二枚の包装材.包装材は100%木綿製で1インチあたり140本の糸が使われている布で,洗濯されていること
3)手術用タオルを敷いたトレイに手術用器具を均等に広げる
4)上記3)で作成した構成物は二重に包装され,滅菌用テープで固定する.
5)BIは器材の中の滅菌が困難と考えられる場所(管状器具やかみ合い部分,ヒンジ部)に設置する.もし指標菌をしみこませたBIの紙片・糸・ワイヤーを滅菌しにくい場所に入れることができない場合には芽胞懸濁液を当該部分にしみこませて生物学的試験を実施してもよい.
3-3. 市販のPCD:SALWAY『コンパクトPCD』
市販のPCDとして、SALWAYのコンパクトPCDを使用しました。コンパクトPCDは、ラパロ鉗子や気腹チューブなどの内腔器材よりも、滅菌抵抗性が高いように設計された市販のPCD(日常の出荷判定用テストパック)です。
コンパクトPCDは細く長い管が内蔵されており、その中を蒸気が通ってインジケータに届くという、内腔器材を模した構造になっています。

3-4. インジケータ:ストリップ型BIとCIを使用
疑似ラパロ鉗子およびコンパクトPCD内の内部にBIを直接設置するために、ストリップ型BIを使用しました。CIは、コンパクトPCDに使用できるプリオンサイクル用インジケータ(SV値:134℃ 18分)を採用しました。

3-5. BIが全死滅しない部分致死サイクルを実施
マスター製品とPCDの滅菌抵抗性は、BIが全死滅しない部分致死サイクルを用いて比較します。部分致死サイクルとは、あえて滅菌条件を悪くして、指標菌の一部が死滅しないサイクルのことです。この部分致死サイクルを実施した時、PCDがマスター製品よりも先に不合格となり、高いBIの生存率を示せば、PCDはマスター製品よりも滅菌抵抗性が高いと言えます。
医療現場における滅菌保証のガイドライン2021(p18)
日常の滅菌処理に使用する出荷可否判定用のテストパックは、以下の優先順位で選定する。①マスター製品にBIおよび/またはCIを設置したもの、②マスター製品に特性が似た製品や模擬製品にBIおよび/またはCIを設置したもの、③市販のPCDにBIおよび/またはCIを設置したもの。②または③を使用する時には、これらが①と同等以上の滅菌抵抗性であることの確認が必要である。「①のマスター製品を用いた出荷可否判定用テストパック」と「③の市販のPCD」の滅菌抵抗性の比較は、①と③を設置したBIが全死滅しない条件である部分致死サイクルにかけて、両者のBIの生残率を比較する。③の市販のPCDのBIが①のマスター製品を用いた出荷可否判定用テストパックのBIよりも高い生残率を示す時に、③の市販のPCDは出荷可否判定用のテストパックに採用できる。
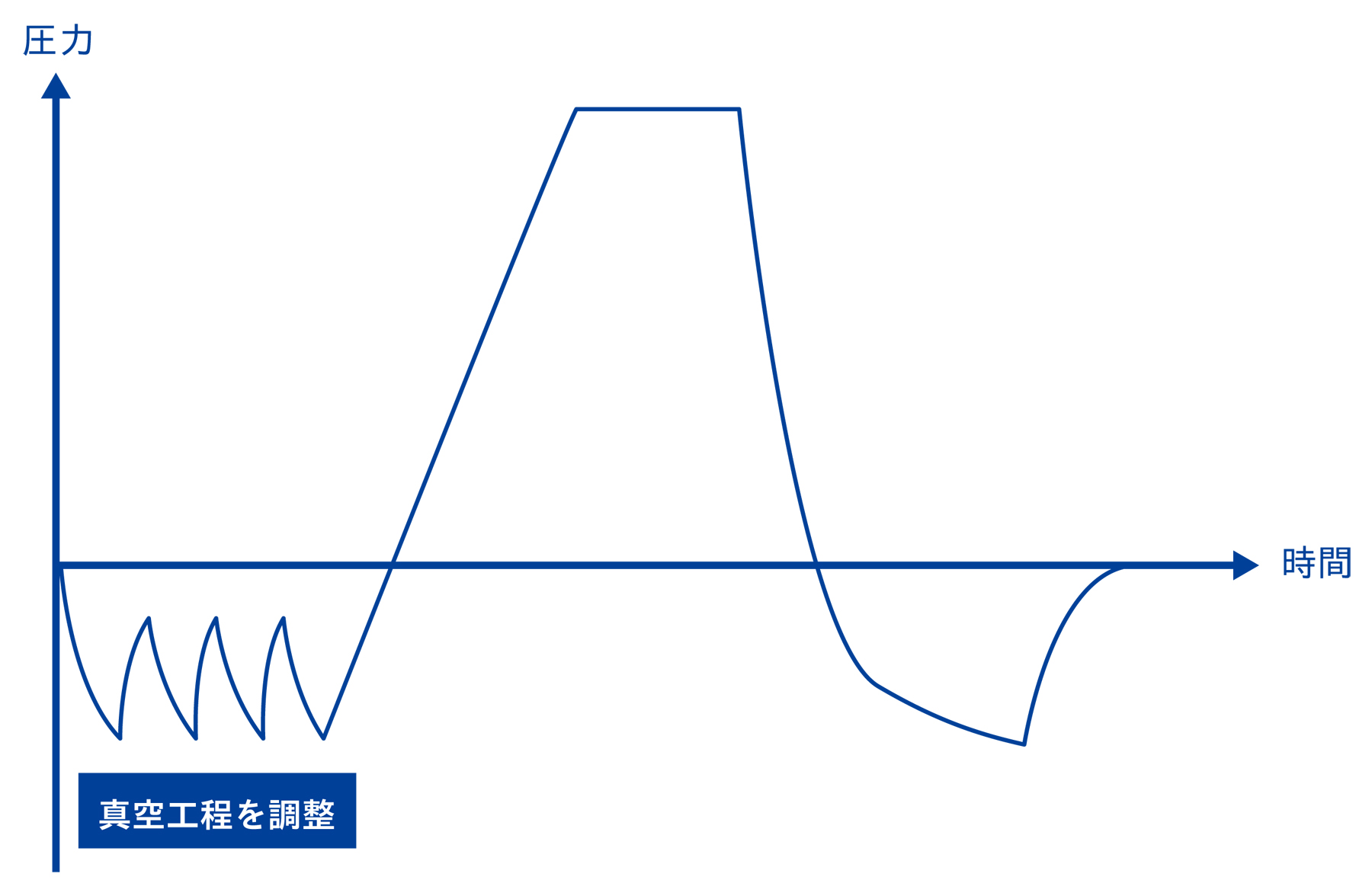
3-6. DIN58921を参考に真空工程を調整して滅菌抵抗性を比較
滅菌条件を悪くする方法として、ドイツ工業規格であるDIN58921を参考にしました。
DIN58921では、開発した医療機器の滅菌確認を行うために、医療機器シミュレーターを開発し、それらの滅菌抵抗性を比較する方法が記載されています。医療機器シミュレーターとは、医療機器の滅菌抵抗性を模倣したPCDのことです。
真空パルス回数や真空到達圧を調整し、意図的に滅菌条件を悪くすることで、器材とPCDの滅菌抵抗性を比較していきます。
4. 検証試験の結果
本試験では、マスター製品とコンパクトPCDの滅菌抵抗性を比較するために、真空パルス回数および真空到達圧を調整しました。それぞれのBIおよびCIの結果を本章で示します。
4-1. CIの結果:滅菌抵抗性は「コンパクトPCD>疑似ラパロ鉗子」
真空パルス回数を3回→2回→1回に変更した時の、CIおよびBIの結果がこちらです。
真空パルスを3回から2回に減らした時に、コンパクトPCD内のCIは不合格を示し、疑似ラパロ鉗子内のCIは合格を示しました。CIの結果においては、コンパクトPCDの方がコンテナ内の疑似ラパロ鉗子よりも滅菌抵抗性が高いことを示唆しています。
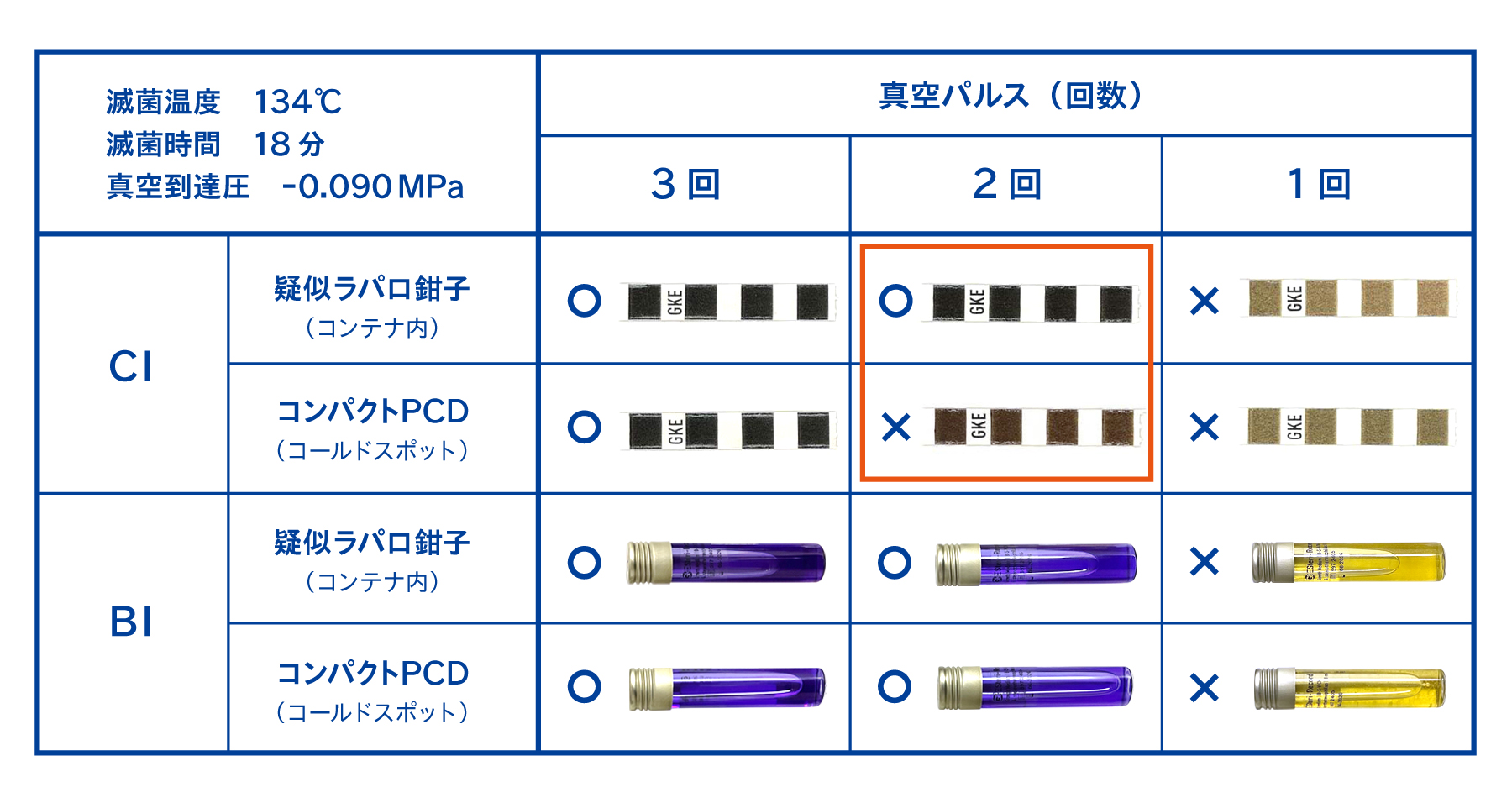
一方のBIでは、真空パルス2回では結果に差がでませんでした。そのため、真空パルス2回で真空到達圧を調整する追加の試験を実施しました(4-2)。
4-2. BIの結果:滅菌抵抗性は「コンパクトPCD>疑似ラパロ鉗子」
真空パルス2回で真空到達圧を-0.070MPa → -0.060MPa → -0.050MPaに変更した時のBIの結果がこちらです。
真空到達圧を-0.070MPaから-0.060MPaに変更した時、コンパクトPCD内のBIは陽性を示し、疑似ラパロ鉗子内のBIは陰性を示しました。BIの結果においても、コンパクトPCDの方がコンテナ内の疑似ラパロ鉗子よりも滅菌抵抗性が高いことが示唆されました。

4-3. コンパクトPCDは重量11.3kgのコンテナ内のラパロ鉗子よりも滅菌抵抗性が高い
CIおよびBIの双方の結果において、本検証におけるマスター製品(重量11.3kgのコンテナに入れた疑似ラパロ鉗子)よりもコンパクトPCDの方が滅菌抵抗性が高いことが示唆されました。
つまり、日常の出荷判定用テストパックとしてコンパクトPCDを使用することで、コンテナで包装したラパロ鉗子の内部での滅菌条件の達成を確認できる、ということです。

5. まとめ
いかがでしたでしょうか。
日常の出荷判定用テストパック(PCD)には、マスター製品と同等以上の滅菌抵抗性が求められます。マスター製品とPCDの滅菌抵抗性を比較するため、DIN58921を参考に、真空工程を調整し意図的に滅菌条件を悪くする方法で検証試験を行いました。
今回の試験では「重量11.3kgのコンテナに入れた疑似ラパロ鉗子」をマスター製品として、SALWAYのコンパクトPCDと滅菌抵抗性を比較しました。真空工程を3回から2回に変更した時に、コンパクトPCD内のCIが先に不合格を示しました。また、真空到達圧を-0.070MPaから-0.060MPaへ変更した時に、コンパクトPCD内のBIが先に陽性を示しました。
CIおよびBIの結果より、「重量11.3kgのコンテナに入れた疑似ラパロ鉗子」よりも、SALWAYのコンパクトPCDの方が滅菌抵抗性が高いことが示唆されました。SALWAYのコンパクトPCDを使用すれば、コンテナ内のラパロ鉗子の内部での滅菌条件の達成を確認することができます。
本記事の内容に関するお問合せは、営業担当またはSALWAYウェブサイトのお問合せフォームよりご連絡下さい。